
미국 FDA와 같은 규제기관과 PDA와 같은 산업 그룹이 수년간 제조 시설의 소독 절차에 관심을 표명하고, EU GMP Annex1 규정이 최근 변경됨에 따라, 실제 제조 시설에서 소독 절차를 확인하기 위해 제약 회사를 대상으로 설문조사를 실시하였으며, 이 결과를 바탕으로 1997년과 2020년 사이의 발전을 살펴본다.
해당 정보는 STERIS의 웹 세미나에서 실시간 여론 조사로 진행되었으며, 총 553명에게 질문이 전송되었고, 180~519명이 해당 질문에 대답하였다.
응답자 중 254명(49%)은 북미에 있었고, 나머지는 남미, 유럽, 아시아, 아프리카 순이었다.

90명(50%)의 응답자는 무균 제조업체에서 근무했으며, 나머지는 비무균제제 또는 의료기기 제조업체에서 근무했다. 기타 화장품 산업, 컨설턴트, 유통업체에서 근무하는 응답자들은 “기타”로 분류되었다.
164명(67%)은 자신의 제조시설이 Annex1의 요구사항을 준수해야 한다고 응답한 반면, 나머지 81명의 응답자는 Annex1의 규제를 받지 않는 현장에서 근무했다.
소독제 적격성평가 방법
소독제 효능 시험은 소독제가 달성할 수 있는 미생물 로그 감소를 기반으로 한다. 그러나, 의약품 제조업체를 위한 로그 감소에 대한 조화된 규제 요구사항은 없다. 따라서, 제조 업체는 자사의 활동과 과거 환경모니터링(EM) 데이터 분석을 기반으로 가장 적절한 로그 감소를 정의해야 한다.
많은 경우 USP<1072>의 로그 감소 기준이 제약 산업에 가장 적합하다. 또한 EN 문서는 식품, 산업, 국내, 기관 및 제약 운영과 같은 다양한 산업에 적용되므로 의약품 제조업체는 다른 유형 또는 표준 조합을 사용하는 것이 논리적이다.

1997년 조사에서는 ATCC 소독제 적격성 여부를 다루지 않았다. 그러나 응답자 중 12명(46%)는 소독제의 유효성을 검증하기 위해 제조 환경에서 분리된 균을 사용한 것으로 나타났다. 나머지 응답자들은 다양한 비환경적 출처의 균을 사용하였다.
현재 규제 지침에 따르면, 광범위한 표준 미생물에 대해 소독제 효능을 입증해야 하는지 여부는 분명하지 않다.
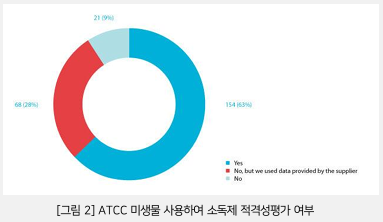
2020년 조사에서는 154명의 응답자(63%)가 표준 미생물을 사용하여 소독제의 적격성을 확인했다. 그러나 응답자 68명(28%)은 소독제 공급업체가 생성한 데이터를 사용했다.
테스트에 사용된 쿠폰이 제조업체 클린룸 표면을 대표하고 최종 사용자의 소독제 정책을 준수하는 자격을 갖춘 경우, 의약품 제조업체는 공급업체가 생성한 데이터를 사용할 수 있다.
소독제 순환
1997년 조사에서는 25명(96%)의 응답자가 소독제를 순환적으로 사용했으며, 그 중 매주 9명(35%), 매월 11명(42%)이 순환 사용하는 것으로 나타났다. 1997년 조사에서 “소독제 순환사용(Rotation of disinfectant)”이라는 용어는 하나의 살포제(sporcide)를 포함하거나 포함하지 않은 두 개의 소독제(disinfectant)를 의미한다. 소독제 순환 응답자 중 79명(51%)은 과거 EM 데이터 검토를 기반으로 소독제 교체의 타당성을 확인했다. 이와 반대로, 나머지는 특정 또는 국가 규정을 준수하기 위해 소독제를 교체하였다. 이는 살포자(sporcide)와 함께 필요한 소독제(disinfectant) 수에 대한 규제 지침이 일치하지 않는다는 것을 시사한다.
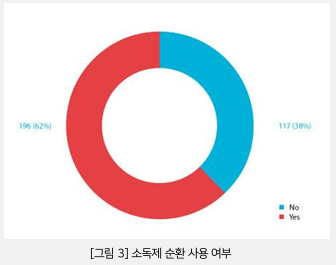
이에 비해 2020년 조사에서는 190명(68%)의 응답자가 소독제(살포제 미포함)를 교체하는 것으로 나타났다. 이러한 감소는 클린룸 바이오버든이 과거 EM 데이터 분석에 의해 제어되고 뒷받침될 때, 소독제 순환이 항상 필요하지 않을 수 있음을 보여준다.
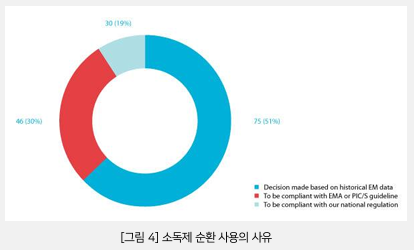
응답자 중 79명(51%)은 과거 EM 데이터 검토를 기반으로 소독제 교체의 타당성을 확인했다. 이와 반대로, 나머지는 특정 또는 국가 규정을 준수하기 위해 소독제를 교체하였다. 이는 살포자(sporcide)와 함께 필요한 소독제(disinfectant) 수에 대한 규제 지침이 일치하지 않는다는 것을 시사한다.
청소 및 소독 빈도 정의
1997년 조사에서는 응답자 중 19명(73%)이 살포제(Sporcide)를 사용하는 것으로 나타났으며, 이들은 매일, 매주 또는 매월 청소 절차에 살포제(Sporcide)를 포함한다고 답했다.
청소 및 소독 빈도는 클린룸 등급, 클린룸 내 활동, 표면 위치(개방형 프로세스 근처 또는 무균 구역), 작업자의 개입, 과거 EM 데이터 등 여러 요인에 따라 달라진다.
2020년 설문조사 응답자 중 98명(34%)은 철저한 미생물 위험 평가를 바탕으로 청소 및 소독 빈도가 타당하다고 답변했다. 이에 비해 72개(26%)는 과거 EM 데이터와 기준 초과 횟수를 근거로 청소 및 소독 빈도를 정의했다. 마지막으로 102개(36%)는 클린룸 등급 분류에 따라 청소 및 소독 빈도를 정의한다.
잔류물(Residue) 제거 절차
1997년 조사 응답자 중 13명(50%)는 잔류물을 제거하기 위해 해당 부위를 린싱하는 것으로 나타났다. 2020년 설문조사에 따르면 응답자 중 17명(67%)이 클린룸에 쌓인 잔류물을 제거하는 절차를 갖고 있는 것으로 나타났다. 2020년 설문 응답자들은 잔류물 축적 제거를 주로 제품과 접촉하지 않는 표면의 육안 검사를 기반으로 한다고 밝혔다. 82명(32%)은 허용 가능한 잔류물 축적에 대한 분석 결과를 기준으로 잔류물 제거 빈도를 정의하였다.

결론
지난 20년 동안 기술과 연구의 발전은 규정과 산업 표준의 변화뿐만 아니라 청소와 소독 방법의 개선으로 이어졌다.
이러한 변화와 발전을 이해함으로써 제조시설은 깨끗하고 위생적인 GMP 클린룸을 유지하기 위한 모범 사례를 최신으로 유지하여 제조된 제품의 품질과 안전을 보장할 수 있다. 이러한 이해는 또한 제조시설이 개선해야 할 부분을 식별하고 장비와 공정에 대한 투자에 대한 정보에 입각한 결정을 내리는 데 도움을 줄 수 있다.
'My Job > Technical for Pharmaceutical' 카테고리의 다른 글
| Taking a Data-Centric Approach to Computer Systems Validation (1) | 2023.12.28 |
|---|---|
| Visual inspection 최적화는 A.I를 이용하여 가능하다. (0) | 2022.11.29 |
| Sterility (멸균)에 대한 정리 및 개념 (0) | 2022.11.29 |
| PUPSIT and the Annex 1 Revision (0) | 2022.11.29 |
| Plasma (플라즈마) 를 이용한 vial의 CCIT 및 진공도 확 (1) | 2022.11.29 |